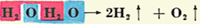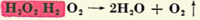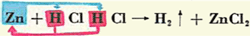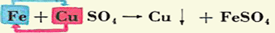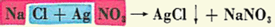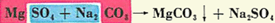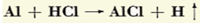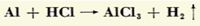جرم اتمی
عدد جرمی نشان دهنده مجموع پروتن ها و نوترون های یک اتم است و از جایی
که جرم پروتون و نوترون با هم یکی نیست عدد جرمی نمیتونه ملاک خوبی برای
شیمیدانها در زمینه هایی مثل حل مساله ، محاسبه بازده و... باشه پس باید
به دنبال راهی بود که بتوان به هر اتم، جرمی رو نسبت داد اما چون اتم بسیار
کوچک هست حتی با ترازو های بسیار دقیق هم نمیتوان جرمی رو به اتم نسبت
داد ولی میتونیم نسبت جرم دو اتم رو بگیم از این رو میتوان عددی رو به عنوان
جرم به یک اتم نسبت بدیم و جرم بقیه اتم ها رو از روی اون حساب کنیم.
به جرم بدست امده با این روش جرم اتمی نسبی میگویند. تا بحال استاندادهای
مختلفی برای تنظیم جرم بیان شده مثلا در ابتدا جرم اتم هیدروژن را یک فرض
کرده و جرم بقیه عناصر را از روی اون حساب کردند اما بعد از کشف ایزوتوپ ها
فیزیکدانان تصمیم گرفتند که واحد جرمی رو یک-شانزدهم جرم فراوانترین ایزوتوپ
اکسیژن یعنی
اندکی تفاوت پیدا کرد.
سرانجام در سال 1961 فیزیکدانان و شیمیدانان به توافق رسیدند که واحد جرم
اتمی را یک-دوازدهم جرم
جرم اتمی را با
مول و عدد اووگادرو
یک مول از هر عنصر (ترکیب) برابر با جرمی از ان عنصر (ترکیب) بر حسب گرم
است که از لحاظ عددی برابر جرم اتمی ان است.
تعداد اتم ها در هر مول از هر ماده با هم برابر است به این تعداد عدد اووگادرو گویند
و با
مثال:
جرم واحد کربنی را بر حسب گرم محاسبه کنید .
طبق تعریف جرم هر اتم
پس اگر به تعداد عدد اووگادرو اتم
گرم خواهد شد پس یه تناسب میبندیم داریم:
ایزوتوپ ها
عنصر معمولا به چند صورت در طبیعت وجود دارد. میزان فراوانی هر ایزوتوپ مقدار
مشخص و ثابتی ست برای محاسبه جرم اتمی میانگین یک عنصر.
با دانستن فراوانی ایزوتوپ های اون از فرمول زیر استفاده میکنیم:
که M بزرگ ، جرم اتمی هر ایزوتوپ و f ، فراوانی اون ایزوتوپ هست.
فرمولهای شیمیایی
- فرمول ساده یا تجربی یا امپریک : فرمول تجربی ساده ترین نسبت عددی صحیح
بین اتم های تشکیل دهنده هر مولکول ان ترکیب را نشان میدهد.
برای مثال فرمول تجربی اب اکسیژنه (
- فرمول مولکولی : این فرمول تعداد واقعی اتم ها در ملکول را بیان میکند و همواره
مضرب صحیحی از فرمول تجربی است.
برای مثال فرمول ملکولی اب اکسیژنه
حالا برای محاسبه فرمول مولکولی یه ترکیب اول اون رو انالیز میکنند تا درصد عناصر
سازنده مشخص بشه بعد این درصد ها رو بر جرم مولی عنصر مذکور تقسیم میکنند
و سپس این اعداد رو به کوچکترین عدد بدست امده تقسیم میکنند اعداد حاصل باید
صحیح باشند اگر نبود تمام اعداد رو در یک عدد ضرب میکنیم تا اعداد صحیح شوند ،
اعداد بدست امده بیانگر فرمول تجربی ترکیب هست.
حالا اگر جرم فرمول مولکولی رو بر جرم فرمول تجربی تقسیم کنیم ضریبی بدست میاد
که اگر این ضریب رو در فرمول تجربی ضرب کنیم فرمول مولکولی حاصل میشه.
برای تفهیم موضوع به مثال زیر توجه کنید
مثال:
تجزیه عنصری بنزوات متیل نشان داده است که این ترکیب به ترتیب از عناصر کربن ،
هیدروژن و اکسیژن با درصد های جرمی 70.58% ، 5.93% ، و 23.58% تشکیل
شده است. مطالعه خواص فیزیکی ان نشان داده است که جرم فرمول مولکولی ان
136 است.فرمول مولکولی بنزوات متیل را بیان کنید .
خوب داریم :
همه رو به کوچکترین عدد حاصل تقسیم میکنیم
میشه
پس فرمول تجربیش میشه
حالا اگر جرم فرمول مولکولی رو به جرم فرمول تجربی تقسیم کنیم میشه 2
پس فرمول واقعیش